
Europäischer Bevollmächtigter
Qserve agiert als Ihr vertrauenswürdiger EU-Rechtsvertreter für Medizinprodukte und IVDs und gewährleistet die Einhaltung der MDR/IVDR-Vorschriften sowie einen reibungslosen Zugang zum europäischen Markt.
Bevollmächtigter der EU (EC REP)
Die Europäische Union verlangt von jedem Nicht-EU-Hersteller, der seine Produkte in der EU verkaufen will, dass er einen alleinigen Bevollmächtigten (EC REP) benennt. Der Europäische Bevollmächtigte vertritt Ihr Unternehmen bei den nationalen Behörden und registriert Ihre Produkte vor der Vermarktung im elektronischen System. Er ist das Bindeglied zwischen einem Hersteller und einer nationalen zuständigen Behörde. Der Name und die registrierte Adresse sind auf allen produktbezogenen Kennzeichnungen zu verwenden.
Mit Qserve als Ihrem EU-Bevollmächtigten sichern Sie sich einen strategischen Partner, der Ihre Interessen auf dem europäischen Markt schützt, während Sie sich auf Innovation und Wachstum konzentrieren.

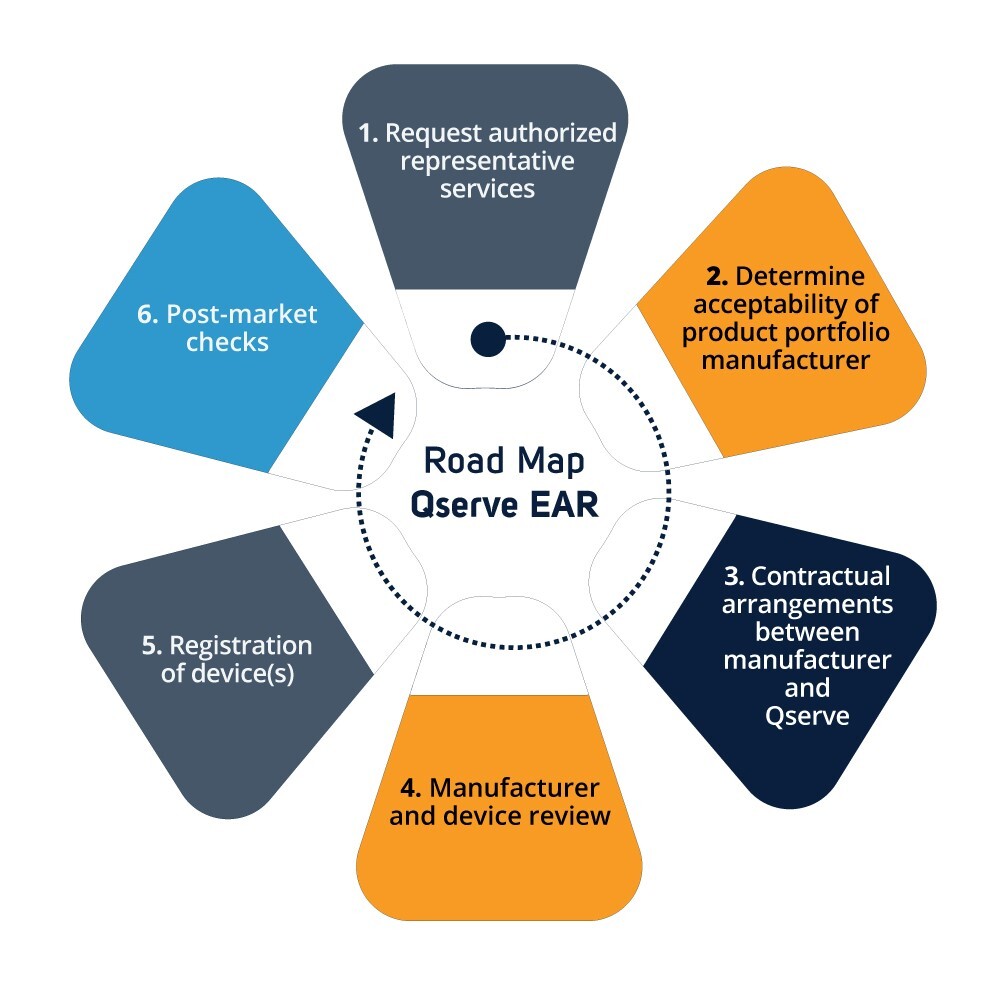
Zuständigkeiten des EU-Vertreters
-
Zugang und Verfügbarkeit Ihrer aktuellsten technischen Unterlagen
-
Handeln innerhalb von 24 Stunden im Falle von Zwischenfällen und der Meldung von Sicherheitskorrekturmaßnahmen (FSCA) im Feld.
-
Erste Anlaufstelle für die zuständige Behörde
Aufgrund der verschärften Haftung nach der MDR/IVDR hat Qserve seine Prozesse und Systeme aktualisiert, um den Anforderungen des Artikels 11 gerecht zu werden. Qserve prüft Ihre technische Dokumentation und bietet bei Bedarf Unterstützung an. Gemeinsam stellen wir sicher, dass Ihre Dokumentation den Vorschriften entspricht. Sobald dies geschehen ist, werden Ihre Medizinprodukte registriert.
Je nach Klassifizierung des Produkts kann die Art der Überprüfung variieren. Bei Produkten der Klasse I muss der Hersteller die Konformität mit der MDR/IVDR selbst erklären. Bei Medizinprodukten der Klassen II und III ist eine benannte Stelle beteiligt, und erst nach der Genehmigung (CE-Zertifikat) kann die EAR die Produkte registrieren.
Rechtmäßig niedergelassen in der EU
Qserve ist eine vollständig registrierte und konforme juristische Person in der EU, die alle MDR- und IVDR-Anforderungen für bevollmächtigte Vertreter erfüllt.
Offizielle Kontaktstelle für Regulierungsbehörden
Wir agieren als Ihr formell ernannter EU-Vertreter und dienen als direkte Verbindung zwischen Ihrem Unternehmen und den zuständigen europäischen Behörden.
Unabhängiger und vertrauenswürdiger Partner
Als unabhängiges Unternehmen bietet Qserve zuverlässige und unvoreingenommene Unterstützung, wobei die Einhaltung von Vorschriften und der Markterfolg stets im Vordergrund stehen.
Beratung zu Registrierungsstrategien
Wir führen Sie durch die effizientesten regulatorischen Wege für die CE-Kennzeichnung und den EU-Marktzugang.
Gewährleistung der Einhaltung aller EU-Vorschriften
Wir unterstützen Sie bei der Erfüllung der in der EU-Gesetzgebung festgelegten Verpflichtungen, einschließlich Überwachung, Dokumentation und Registrierung.
Erfahrener Partner für globale Hersteller
Qserve hat Hunderte von Herstellern - von Start-ups bis hin zu globalen Unternehmen - bei der Navigation durch die komplexe EU-Regulierungslandschaft unterstützt.

Laden Sie die Broschüre EU-Vertreter herunter und erfahren Sie, wie Qserve als Ihr EU-Vertreter agieren kann.
Der EU-Vertreter (EC Rep | EAR) vertritt Ihr Unternehmen bei den nationalen Behörden und registriert Ihre Medizinprodukte vor dem Inverkehrbringen im elektronischen System.
Neueste Blogs
.png)
Erfahren Sie mehr über die Aufgaben, Zuständigkeiten und rechtlichen Anforderungen eines FDA-Beauftragten in den USA.

Entdecken Sie, wie Regulatory-Intelligence-Plattformen Zeit sparen, Fehler reduzieren und Compliance zum strategischen Vorteil machen.
.png)
Planen Sie die Einreichung Ihrer klinischen Prüfung in Deutschland: Sorgen Sie für Klarheit in den Abläufen und für MDR-konforme Dokumente, um Verzögerungen oder Fragen seitens der Europäischen Kommis...
